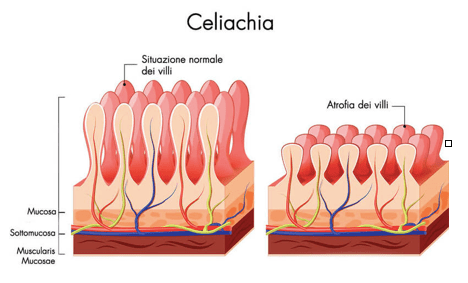
La celiachia è una malattia multifattoriale. Perché si manifesti sono necessari, ma non sufficienti, due determinanti: la presenza di glutine (fattore ambientale) e la predisposizione genetica (fattore genetico), cioè occorre che siano presenti due molecole nel sistema immunitario, HLA-DQ2 e HLA-DQ8, in grado di legare in modo specifico frammenti di glutine e di presentarli alle cellule immunitarie, che non riconoscendole, scatenano le reazioni. Quindi le cellule del sistema immunitario, innescate dal contatto con il glutine, attaccano la mucosa dell’intestino tenue, distruggendo i villi (piccole protuberanze a forma di dito responsabili dell’assorbimento dei vari nutrienti) e determinando, a lungo andare, malassorbimento e malnutrizione.
Solo il 30% della popolazione mondiale con queste sequenze finisce per presentare la malattia. Che cosa ne promuove lo sviluppo? Il trigger non lo conosciamo ancora, è il tassello che manca per prevenire e quindi curare definitivamente i celiaci.
In aggiunta alla predisposizione genetica e all’esposizione al glutine, la perdita di funzione della barriera intestinale, una risposta immunitaria innata pro-infiammatoria innescata dal glutine, una risposta immunitaria adattativa inappropriata ed un microbioma intestinale squilibrato, sembrano essere tutti ingredienti chiave della “ricetta” della autoimmunità celiaca.
Attualmente si stima che la celiachia interessi circa l’1% della popolazione generale, con una prevalenza riportata maggiormente tra le donne e con l’eccezione di aree che mostrano una bassa frequenza di geni predisponenti ed un basso consumo di glutine (ad es. l’Africa subsahariana e il Giappone). Può presentarsi a qualsiasi età, con una varietà di sintomi e manifestazioni: classicamente si presenta nella forma intestinale, con sintomi come gonfiore, diarrea, anemia, scarsa capacità di concentrazione, affaticabilità, cefalea, osteopenia.
Ma cosa è il glutine?
Il glutine è un artefatto umano, una molecola complessa, resistente alla trazione, che deriva dall’impasto di farina e acqua: il nome, non a caso, deriva dall’inglese glue, cioè colla. Alla base del glutine sono due proteine, nella farina separate: gliadina e glutenina che, per effetto combinato dell’acqua e dell’azione meccanica dell’impastare, danno origine alla massa reticolare che chiamiamo glutine.
La sua funzione è rendere gli alimenti più palatabili, grazie a viscoelasticità (vedi la pizza) e sofficità (pane, torte), data dalla capacità di trattenere l’aria, che origina dalla fermentazione dei lieviti.
Introdotti 10.000 anni fa durante la transizione da uno stile di vita nomade agli insediamenti agricoli, i cereali contenenti glutine sono un’aggiunta recente alla dieta umana. Per di più, il glutine non è digeribile dal nostro intestino, benché venga consumato cronicamente in quantità significative. Ecco perché dopo aver mangiato la pizza e la pasta ci si sente “gonfi”: risultano difficili da digerire. La prolamina, in particolare, è una delle frazioni proteiche che costituiscono il glutine ed è la responsabile dell’effetto tossico nel celiaco.
Malattie associate alla celiachia
Come qualsiasi altra malattia autoimmune, la malattia celiaca ha una forte componente ereditaria, come testimoniato dalla sua elevata incidenza familiare (circa 10-15%). La MC può essere associata a diverse malattie autoimmuni e idiopatiche tra cui la dermatite erpetiforme, diabete mellito di tipo 1, tiroidite di Hashimoto, malattia di Addison, malattie cromosomiche (sindrome di Down, Turner e William), malattie neurologiche etc. L’importanza di diagnosticare la MC associata a queste malattie concomitanti è duplice, poiché una dieta senza glutine è in grado di risolvere i sintomi, prevenire complicanze e agire favorevolmente su alcune delle patologie ad essa associate.
Diagnosi
Diagnosticare la celiachia può essere difficile poiché i sintomi possono variare in modo significativo da paziente a paziente. Tuttavia, negli ultimi anni ci sono stati cambiamenti significativi relativi alla diagnosi di questa condizione. Ciò è stato principalmente attribuito alla maggiore disponibilità di test di screening sensibili e specifici, che consentono l’identificazione dei gruppi a rischio e hanno portato ad un importante aumento delle diagnosi in tutto il mondo.
La metodologia gold standard è rappresentata dalla combinazione di biopsia duodenale, che rileva alterazioni della mucosa e positività dei test sierologici (anticorpi anti-tTG, anticorpi anti-endomisio EmA e anticorpi peptide gliadina deamidato DGP). L’attuale algoritmo di diagnosi si basa sulla “regola del 4 su 5”, che indica che quattro su cinque dei seguenti criteri sono sufficienti per stabilire la diagnosi di celiachia: (1) segni e sintomi tipici (diarrea e malassorbimento); (2) positività anticorpale; (3) positività HLA-DQ2 e/o HLA-DQ8; (4) danno intestinale (cioè atrofia dei villi e lesioni minori); e (5) risposta clinica alla gluten-free diet (GFD).
Trattamento
Attualmente, l’unico trattamento efficace disponibile per la malattia celiaca è una GFD rigorosa per tutta la vita, vale a dire l’esclusione dei grani che contengono glutine e dei prodotti da questi derivati. Gli unici cereali concessi al celiaco, poiché naturalmente privi di glutine, sono riso, mais, sorgo, amaranto, quinoa, fonio, teff e grano saraceno.
Questo regime alimentare porta alla risoluzione dei sintomi intestinali ed extra-intestinali, alla negatività degli autoanticorpi e alla ricrescita dei villi; miglioramenti che si verificano in genere entro giorni o settimane. Inoltre, offre un effetto protettivo parziale nei confronti di numerose complicanze.
Tuttavia, questi cruciali vantaggi sono accompagnati da alcuni svantaggi, tra cui un impatto negativo sulla qualità della vita, problemi psicologici, paura della contaminazione involontaria con il glutine, possibili carenze di vitamine e minerali, sindrome metabolica, un aumento del rischio cardiovascolare e spesso grave costipazione. La maggior parte di questi inconvenienti può essere superata istruendo il paziente sui rischi di un regime senza glutine incontrollato e seguendo raccomandazioni nutrizionali di un dietologo con esperienza in celiachia. Da un punto di vista psicologico, il supporto di un professionista potrebbe essere molto utile per accettare la malattia e meglio convivere con essa.
Implicazioni nutrizionali della GFD
L’adeguatezza nutrizionale della GFD rimane controversa, dato che evidenze suggeriscono che essa sia squilibrata dal punto di vista nutrizionale. In effetti, il grano è fonte di ferro, folati e vitamine del gruppo B (tiamina, riboflavina e niacina), oltre che di proteine. Verosimilmente, i prodotti senza glutine hanno un basso contenuto di questi nutrienti rispetto ai loro equivalenti contenenti glutine. Pazienti con MC potrebbero quindi presentare vari stati di carenze, tra cui anemia, osteopenia e osteoporosi.
Tra il 20% e il 38% dei pazienti celiaci manifestano carenze nutrizionali. In particolare, il 12%-69% mostra carenze di ferro, più frequentemente negli adulti che nei bambini; l’8%-41% mostra carenza di vitamina B12 e circa il 31% presenta basse concentrazioni di ferritina.
Il ferro è un micronutriente essenziale per un’adeguata produzione di globuli rossi, è implicato nel metabolismo ossidativo, attività enzimatiche e risposte immunitarie cellulari. Cambiamenti nella densità minerale ossea, inclusa l’osteopenia o l’osteoporosi (che interessano circa il 70% dei pazienti alla diagnosi), sono correlati ad un assorbimento alterato di calcio e vitamina D3.
C’è da dire che le carenze nutrizionali del paziente celiaco sono attribuibili sicuramente al malassorbimento dovuto al danneggiamento della mucosa duodenale, ma anche come risultato di una scarsa aderenza ad una dieta senza glutine bilanciata; non è chiaro in quale percentuale influenzi ciascun fattore. La GFD richiede una significativa educazione, motivazione e follow-up del paziente, ecco perché si ritiene che la partecipazione di nutrizionisti nella gestione della malattia sia necessaria per educare alla dieta senza glutine, renderla più bilanciata, nonché fortificarla in quei micronutrienti che potrebbero essere carenti.
Il futuro si apre a nuove strategie terapeutiche e preventive, che dovrebbero migliorare la qualità della vita del paziente e aprire la strada a una cura definitiva per questa malattia.
Bibliografia
– Caio G, De Giorgio R, Volta U. Coeliac disease and dermatitis herpetiformis. Lancet. 2018 Sep 15;392(10151):916-917. doi: 10.1016/S0140-6736(18)31486-7. PMID: 30238885.
– Caio G, Volta U, Sapone A, et al. Celiac disease: a comprehensive current review. BMC Med. 2019;17(1):142. Published 2019 Jul 23. doi:10.1186/s12916-019-1380-z
– Catassi C, Fasano A. Celiac disease diagnosis: simple rules are better than complicated algorithms. Am J Med. 2010 Aug;123(8):691-3. doi: 10.1016/j.amjmed.2010.02.019. PMID: 20670718.
– Corazza GR, Andreani ML, Biagi F, Corrao G, Pretolani S, Giulianelli G, Ghironzi G, Gasbarrini G. The smaller size of the ‘coeliac iceberg’ in adults. Scand J Gastroenterol. 1997 Sep;32(9):917-9. doi: 10.3109/00365529709011202. PMID: 9299671.
– Leffler DA, Green PH, Fasano A. Extraintestinal manifestations of coeliac disease. Nat Rev Gastroenterol Hepatol. 2015 Oct;12(10):561-71. doi: 10.1038/nrgastro.2015.131. Epub 2015 Aug 11. PMID: 26260366.
– Moreno ML, Cebolla Á, Muñoz-Suano A, Carrillo-Carrion C, Comino I, Pizarro Á, León F, Rodríguez-Herrera A, Sousa C. Detection of gluten immunogenic peptides in the urine of patients with coeliac disease reveals transgressions in the gluten-free diet and incomplete mucosal healing. Gut. 2017 Feb;66(2):250-257. doi: 10.1136/gutjnl-2015-310148. Epub 2015 Nov 25. PMID: 26608460; PMCID: PMC5284479.
– Nestares T, Martín-Masot R, Labella A, Aparicio VA, Flor-Alemany M, López-Frías M, Maldonado J. Is a Gluten-Free Diet Enough to Maintain Correct Micronutrients Status in Young Patients with Celiac Disease? Nutrients. 2020 Mar 21;12(3):844. doi: 10.3390/nu12030844. PMID: 32245180; PMCID: PMC7146183.
– Roos S, Kärner A, Hallert C. Psychological well-being of adult coeliac patients treated for 10 years. Dig Liver Dis. 2006 Mar;38(3):177-80. doi: 10.1016/j.dld.2006.01.004. Epub 2006 Feb 7. PMID: 16461026.
– Silano M, Vincentini O, De Vincenzi M. Toxic, immunostimulatory and antagonist gluten peptides in celiac disease. Curr Med Chem. 2009;16(12):1489-98. doi: 10.2174/092986709787909613. PMID: 19355902.
– Singh P, Arora S, Singh A, Strand TA, Makharia GK. Prevalence of celiac disease in Asia: A systematic review and meta-analysis. J Gastroenterol Hepatol. 2016 Jun;31(6):1095-101. doi: 10.1111/jgh.13270. PMID: 26678020.
– Volta U, Caio G, Stanghellini V, De Giorgio R. The changing clinical profile of celiac disease: a 15-year experience (1998-2012) in an Italian referral center. BMC Gastroenterol. 2014 Nov 18;14:194. doi: 10.1186/s12876-014-0194-x. PMID: 25404189; PMCID: PMC4236812.
AUTORE: Angelica Rossi Freelance e Biologa di Scienze Salute e Benessere