È noto che la dieta modula drasticamente la composizione del microbiota intestinale. A causa della notevole complessità delle risposte allo stress (dall’intestino permeabile all’aumento del catabolismo e della depressione), è impossibile definire piani alimentari standard. Tuttavia, alcuni dati sperimentali ottenuti da studi scientifici mostrano alcuni risultati interessanti, indicando che il microbiota agisce come un organo endocrino (ad esempio secernendo serotonina, dopamina o altri neurotrasmettitori) e può controllare l’asse HPA (ipotalamo-ipofisi-surrene).
Lo stress è la risposta del corpo a qualunque richiesta. Stando a questa definizione lo stress è parte fondamentale dell’essere vivente ma il punto è fare in modo che esso non ci travolga. Le manifestazioni sono molto variabili e soggettive: stanchezza, irritabilità, difficoltà a staccare e rilassarsi, essere sempre all’ultimo minuto, insonnia, alvo non regolare con meteorismo, palpitazioni e cefalea. Chiunque abbia subito un trauma (fisico, psichico o biologico) ha una massiccia attivazione del sistema nervoso simpatico con secrezione a cascata di ormoni dello stress (cortisolo, adrenalina e noradrenalina) attraverso l’asse HPA (ipotalamo-ipofisi-surrene). Il cortisolo ad esempio, in elevate quantità, inibisce l’ippocampo temporaneamente ed a lungo termine può condurre alla morte delle cellule dell’ippocampo, zona cerebrale colpita nell’Alzheimer). Inoltre l’iperattivazione dell’asse dello stress HPA altera l’integrità dell’epitelio intestinale, la motilità intestinale e la composizione del microbiota intestinale (livelli elevati di noradrenalina intestinale incrementano la crescita e la patogenicità dei batteri). A breve termine (fase acuta), lo stress può ridurre l’appetito in quanto viene temporaneamente rilasciata l’adrenalina che aiuta ad innescare uno stato fisiologico accelerato che mette temporaneamente in pausa il mangiare. Ma se lo stress persiste (fase cronica), è una storia diversa perchè viene rilasciato cortisolo in elevate quantità, aumentando così l’appetito. Inoltre il disagio fisico o emotivo sembra influenzare le preferenze alimentari, incentivando l’assunzione di cibo ad alto contenuto di grassi, zuccheri o entrambi a causa dell’azione della “grelina” (l’ormone della fame).
Una corretta funzione della barriera intestinale è fondamentale quindi per mantenere la condizione fisiologica dell’organismo. In condizioni di stress (anche uno sforzo fisico) la temperatura corporea aumenta e il sangue si accumula dal tratto gastrointestinale ai muscoli e agli organi periferici come il cuore e i polmoni. La ridistribuzione del flusso sanguigno lontano dall’intestino insieme al danno termico alla mucosa intestinale può causare la rottura della barriera intestinale, seguita da una risposta infiammatoria. Inoltre, un prolungato esercizio intenso aumenta gli ormoni dello stress e la traslocazione dei lipopolisaccaridi (LPS) nel tratto gastrointestinale, che innesca risposte immunitarie che spesso si traducono in un aumento delle citochine pro-infiammatorie e della permeabilità intestinale. Quest’ultima può essere aggravata dall’aumentata produzione di ROS (stress ossidativo cellulare) e dall’alterazione della composizione del microbiota intestinale (disbiosi). Inoltre, il tratto gastrointestinale risponde allo stress rilasciando ormoni come GABA, neuropeptide Y (NPY) e dopamina che possono causare disturbi gastrointestinali, ansia, depressione. Al contrario, la produzione di butirrato e propionato da parte del microbiota può aumentare la resistenza transepiteliale, che migliora la funzione di barriera intestinale e riduce l’infiammazione.
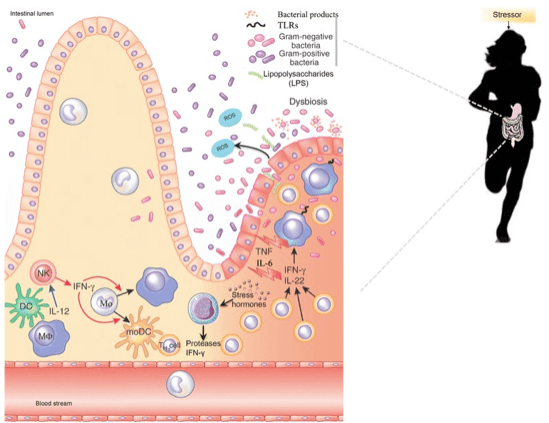
L’insieme delle prove scientifiche indicano che il microbiota intestinale e i microbiomi associati possono influenzare i processi patogeni e quindi l’insorgenza e la progressione di varie malattie neurodegenerative, tra cui il Parkinson, l’Alzheimer e la sclerosi multipla.
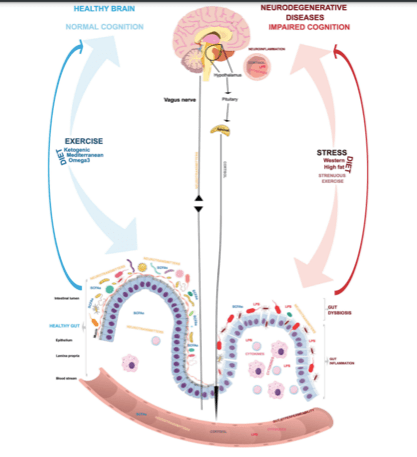
Inoltre prove crescenti indicano che i pazienti con gravi disturbi mentali, tra cui depressione maggiore, disturbo bipolare e schizofrenia, presentano varie alterazioni del microbiota intestinale e un aumento della permeabilità intestinale con una disregolazione dell’asse HPA. Tale asse può essere influenzato e quindi alterato dalla produzione di corticosterone ileale da parte di varie specie microbiche; invece alcuni metaboliti rilasciati da vari microbi, ad esempio gli acidi grassi a catena corta, possono attenuare e ristabilire la risposta dell’asse HPA.
Altro fattore che dimostra la correlazione tra il nostro intestino e cervello è lo stress prenatale materno, il quale risulta essere associato allo sviluppo fisico e alla salute del bambino, nonché al funzionamento e al comportamento psicologici. I neonati di madri con elevato stress cumulativo (cioè, alto stress riportato e alte concentrazioni di cortisolo) durante la gravidanza avevano un’abbondanza relativa significativamente più alta di gruppi proteobatterici (noti per contenere agenti patogeni) e una minore abbondanza relativa di batteri lattici e Bifidobatteri, complessivamente caratteristiche di un potenziale aumento del livello di infiammazione.
In conclusione per prevenire tali condizioni è utile attivare un’inclinazione verso il sistema nervoso parasimpatico attraverso l’attivazione del nervo vago, lo strumento con cui il nostro cervello si connette al resto del corpo. La personalizzazione del trattamento prevede quindi: un’osservazione accurata del paziente, compreso il suo aspetto, Un’anamnesi molto accurata comprendente abitudini, stile di vita, psichismo, antecedenti medici e chirurgici, antecedenti genetici-familiari, carattere e attività svolte. Tutto ciò servirà per poter indicare il giusto trattamento alimentare e fitoterapico al fine di poter ristabilire il fisiologico funzionamento del nostro metabolismo e di poter prevenire condizioni gravemente patologiche e dannose.
Referenze
– Clark A. e Mach N. Exercise-induced stress behaviour, gut-microbiota axis and diet: a systematic review for athletes, J Int Soc Sports Nutr, 2016.
– Gubert C., Kong G., Renoir T., J.Hannan A. Exercise, diet and stress as modulators of gut microbiota: implications for neurodegenerative diseases; Neurobiology of Diseases, Vol 134, 2020.
– Misiak B., Loniewski I., Marlicz W., Frydecka D., Szulc A., Rudzki L., Samochoweic J. The HPA axis dysregulation in severe mental illness: Can we shift the blame to gut microbiota? Progress in Neuro-Psychopharmacology and Biological Psychiatry, Vol 102, 2020.
– Zijlmans M.A.C., Korpela K., Riksen-Walraven J.M., De Vos W.M., De Weerth C. Maternal prenatal stress is associated with the infant intestinal microbiota, Psychoneuroendocrinology, Vol 53, 2015.
AUTORE: Claudia Priante Freelance e Biologa di Scienze Salute e Benessere


