Introduzione
L’ osteoporosi è una malattia sempre più diagnosticata nelle donne e negli uomini di tutto il mondo (1). E’ stato detto molto riguardo il ruolo della carenza degli steroidi sessuali nella genesi dell’osteoporosi, in menopausa, ma è anche noto che la mancanza di attività fisica è un fattore di rischio importante (2).
Istologia del tessuto osseo
L’apparato scheletrico assolve sostanzialmente tre funzioni, la prima delle quali è il fornire il supporto architettonico a muscoli e tendini in modo tale da permettere il movimento, la seconda è costituita dal suo ruolo protettivo nei confronti degli organi vitali, mentre la terza consiste nel fornire una riserva organica di calcio rivolta alla stabilizzazione della calcemia, fattore che viene perturbato soprattutto nei periodi di carenza alimentare. Il tessuto osseo è un tessuto dinamico soggetto a numerosi cambiamenti strutturali e funzionali dovuti all’età, all’alimentazione e alle condizioni generali dell’individuo, e plastico: provvede a modulare la propria struttura in seguito a stimoli organici e meccanici. Il tessuto osseo è formato da una parte organica ed una parte inorganica. La parte organica è composta da cellule proprie del tessuto osseo (cellule osteoprogenitrici, osteoblasti, osteociti e osteoclasti che provvedono all’accrescimento, alla produzione e al riassorbimento del tessuto osseo) e da matrice extracellulare (sostanza amorfa e fibre collagene di tipo I). La parte inorganica è costituita da numerosi sali minerali come i fosfati di calcio e magnesio e i citrati di Na, Mn, K.
Le cellule osteoprogenitrici, sono cellule di origine mesenchimale con proprietà staminali: esse possono proliferare e differenziare in osteoblasti. Si trovano nel periostio e nell’endostio: riattivate provvedono alla formazione di nuovo tessuto osseo.
Gli osteoblasti sono i precursori degli osteociti e provvedono alla produzione sia della matrice organica (definita osteoide) che alla deposizione di quella inorganica, hanno quindi funzioni osteogeniche. Producono collagene di tipo I, osteocalcina, osteopontina e sialoproteina dell’osso. Quando gli osteoblasti hanno terminato la formazione dell’osso rimanendo intrappolati all’interno di lacune nella matrice da loro stessi prodotta, diventano osteociti. Essi sono alloggiati nelle lacune ossee dalle quali si dipartono, in ogni direzione, numerosi canalicoli microscopici. Attraverso questi canalicoli i prolungamenti citoplasmatici di osteociti diversi prendono contatto tra di loro tramite giunzioni comunicanti e con capillari sanguigni presenti nei canali ossei, permettendo così scambi metabolici tra gli osteociti stessi e tra osteociti e sangue. Gli osteociti provvedono al mantenimento della matrice extracellulare dell’osso.
Gli osteoclasti sono deputati alla distruzione (riassorbimento) e al rimaneggiamento del tessuto osseo. Quando attivate presentano una faccia citoplasmatica in prossimità dell’osso con caratteristiche increspature molto mobili ed aderiscono alla superficie dell’osso creando un microambiente isolato da quello circostante (zona sigillata) che viene acidificato per l’attivazione successiva di enzimi di derivazione sia lisosomale (proteinasi e fosfatasi) che non lisosomale (metalloproteinasi). Questo processo porta all’erosione della matrice ossea e alla formazione di una depressione definita lacuna di Howship
Il tessuto osseo lamellare costituisce la stragrande maggioranza del tessuto osseo nei mammiferi adulti ed è organizzato in lamelle. Il tessuto osseo lamellare, grazie alla sua composizione chimica e alla sua particolare organizzazione strutturale, ha una forte resistenza alla trazione, alla pressione e alle sollecitazioni meccaniche in generale. Grazie alla sua organizzazione in lamelle, infatti, questo tessuto garantisce una buona resistenza alle sollecitazioni, pur non appesantendo particolarmente lo scheletro. Il tessuto osseo lamellare si divide in tessuto osseo lamellare compatto se è composto prevalentemente da lamelle concentriche complete, come per esempio nelle diafisi, e in tessuto osseo lamellare spugnoso se invece è composto da lamelle incomplete che formano tanti piccoli frammenti incastonati fra di loro (trabecole ossee), come per esempio nelle epifisi. Il tessuto osseo lamellare compatto costituisce le diafisi nelle ossa lunghe, lo strato superficiale delle epifisi, i tavolati delle ossa piatte e in generale riveste tutte le superfici ossee. Le lamelle ossee sono organizzate in strati concentrici a formare gli osteoni, in cui gli osteociti sono posti circolarmente, secondo diverse orbite, intorno a canali, detti canali di Havers, contenenti uno o due piccoli capillari sanguigni. Il numero di lamelle che circonda un singolo canale di Havers può variare da 4 a 20. I vari canali di Havers comunicano tra di loro grazie ad altri canali posti, però, trasversalmente od obliquamente, detti canali di Wolkmann, anch’essi contenenti capillari sanguigni. Le sostanze nutritizie arrivano agli osteociti tramite la rete capillare e distribuite mediante la fitta rete di prolungamenti citoplasmatici che li collegano. Il tessuto osseo lamellare spugnoso è formato da lamelle incomplete associate a formare delle trabecole (come ad esempio nelle epifisi delle ossa lunghe). Questa disposizione spaziale garantisce una migliore resistenza a pressioni multidirezionali, e genera degli spazi intercomunicanti in cui è alloggiato il midollo osseo. Le lamelle sono più o meno intrecciate e di spessore variabile. Gli osteociti sono distribuiti nelle lamelle in maniera disomogenea e con grandezza e forma variabile.
Le superfici esterne dell’osso sono rivestite da una spessa capsula connettivale costituita da tessuto connettivo denso a fibre intrecciate, il periostio. Esso ha il compito di proteggere l’osso e di supportare l’azione trofica mediata dai vasi sanguigni di cui è ricco. Nella faccia esterna del periostio sono presenti poche cellule e molte fibre collagene (strato fibroso), nella faccia interna, invece, vi sono poche fibre, numerosi capillari sanguigni e cellule osteoprogenitrici con potenziale osteogenico (strato osteogenico). Dal periostio si dipartono trasversalmente, verso il tessuto osseo, fibre connettivali, dette fibre di Sharpey, che hanno il compito, addentrandosi nel sistema di lamelle circonferenziali esterne, di fornire un buon sistema di ancoraggio all’osso. Il periostio non è presente nelle articolazioni e nei punti di inserzione di muscoli e legamenti. L’endostio è formato da uno strato di cellule pavimentose e fibre connettivali che ricoprono tutte le superfici interne dell’osso (trabecole ossee dell’osso spugnoso, cavità midollari dell’osso compatto, canali di Havers e di Wolkmann). Le cellule che formano l’endostio hanno un alto potenziale osteogenico.
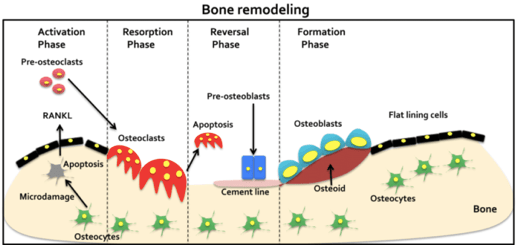
Remodeling ed insorgenza di osteoporosi
L’osso è un tessuto metabolicamente dinamico e la sua durezza dipende dall’equilibrio tra i processi anabolizzanti (apposizione) e processi catabolici (riassorbimento). È noto che la costituzione genetica, la dieta e gli stimoli fisici sono fattori che influenzano il metabolismo osseo, infatti l’apposizione e il riassorbimento osseo sono mediati da ormoni, prodotti cellulari e dalla matrice ossea. Il processo catabolico o riassorbimento osseo, ha la funzione vitale di mantenere stabili i livelli di calcio extracellulare. L’apposizione ossea (la sintesi della matrice ossea e la mineralizzazione) ha due obiettivi principali che consistono nel riposizionare il tessuto osseo perso nel processo catabolico e nel soddisfare le esigenze degli organi adattandole alle condizioni funzionali. Gli squilibri tra questi due processi sono accumulati nel corso della vita, soprattutto a causa di ipocalcemia (12). Come conseguenza della prevalenza del processo catabolico, abbiamo la perdita ossea, soprattutto i fattori inibitori della neoformazione ossea – come quelli associati alla senescenza. Così, i cambiamenti nel metabolismo, nell’assorbimento del calcio e nel profilo ormonale – specialmente nelle donne dopo la menopausa – associati all’inattività fisica, contribuiscono ad uno squilibrio del rimodellamento osseo(13), avendo l’osteoporosi come conseguenza principale(10,11). L’osteoporosi è una malattia metabolica generalizzata, caratterizzata da minore apposizione ossea per insufficienza osteoblastica(5), con riduzione della massa ossea per unità di volume e per eziologia multifattoriale(13). Per quanto riguarda la carenza di ormoni sessuali in menopausa nella genesi dell’osteoporosi, volta cessata la produzione di ormoni sessuali, la massa ossea femminile diminuisce nei primi 10 anni rapidamente e lentamente negli anni successivi(15). Inoltre, in ogni ciclo di rimodellamento troviamo una quantità minore di osso e una quantità maggiore di questo viene riassorbita (14,15). Estrogeni e progesterone agiscono nel rimodellamento osseo(14), ma con meccanismi non ancora del tutto chiari(10). La presenza di recettori degli estrogeni negli osteoblasti e negli osteociti comporta un effetto diretto di questo ormone sul tessuto osseo(16). Per quanto riguarda gli osteoblasti, l’estrogeno aumenta la differenziazione di queste cellule e stimola la sintesi e la mineralizzazione della matrice ossea, regolando l’espressione dei geni che decodificano il collagene di tipo I e le glicoproteine come osteopontina, osteocalcina, osteonectina, e così via(11). Inoltre, l’estrogeno inibisce indirettamente il riassorbimento osseo quando regola la sintesi e i citochine, le prostaglandine e il rilascio dei fattori di crescita(14,15). Il progesterone partecipa anche al metabolismo osseo, in particolare alla sintesi della matrice ossea (11,17). Questo ormone stimola la proliferazione e differenziazione delle cellule osteoprogenitrici (15) e lavora negli osteoblasti regolando la secrezione dei fattori di crescita e stimolando l’apposizione e la mineralizzazione ossea (11). Così, l’osteopenia osservata nella carenza di progesterone sembra derivare dalla diminuzione dell’apposizione ossea (11,18). La riduzione della massa ossea derivata dall’ipogonadismo, è anche in relazione alla diminuzione dell’assorbimento intestinale del calcio. Gli estrogeni hanno un’azione diretta sulla mucosa intestinale e indiretta mediata dalla vitamina D(19). Così, nella carenza di estrogeni ci si aspetta una diminuzione del numero di recettori per la vitamina D nell’intestino (20) e una minore conversione renale della vitamina D inattiva nel suo modo attivo. Di conseguenza, nell’ipogonadismo, si osserva una minore formazione del legame della proteina con il calcio, diminuendone l’assorbimento intestinale(21). Gli ormoni tiroidei T3 e T4 controllano il metabolismo osseo e l’omeostasi minerale degli adulti(22) e il rapporto dell’osteoporosi con la tiroide è stato studiato per molti anni. Gli ormoni tiroidei e gli ormoni sessuali controllano l’espressione genica negli osteoblasti, aumentando l’attività della fosfatasi alcalina e del collagene di tipo I e la produzione di proteine non collageniche (11,17) e fattori di crescita simili all’insulina, aumentando la sintesi della matrice ossea e la mineralizzazione successiva(23). Nelle ipofunzioni tiroidee si riduce il metabolismo generale, che influenza direttamente il reclutamento, la differenziazione, la maturazione e il metabolismo delle cellule responsabili dell’apposizione ossea, mineralizzazione e riassorbimento(24) con conseguente osteoporosi(12). Nell’ipotiroidismo, la diminuzione della mineralizzazione della matrice ossea sembra essere dovuta alla diminuzione dei valori plasmatici di calcio e fosforo (25), una volta che gli ormoni tiroidei (T3 e T4) sono importanti nel trasporto intestinale di calcio e fosforo mediati da 1,25(OH)2D3. I fattori ormonali non sono gli unici coinvolti nella genesi dell’osteoporosi. Si ritiene che la mancanza di attività fisica sia un fattore di rischio, una volta che ampie prove hanno collegato l’inattività fisica alla perdita ossea. E’ stato dimostrato negli esseri umani una deduzione dello 0,9%/settimana del volume osseo trabecolare associato alla diminuzione dell’1,3%/giorno, della forza di contrazione muscolare dopo una prolungata immobilizzazione. L’attività fisica è stata adottata come strategia per prevenire la perdita minerale ossea e per mantenere l’integrità scheletrica, poiché esiste uno stretto rapporto tra attività fisica, densità minerale ossea e massa ossea.
Referenze
1. Notomi T, Okimoto N, Okazaki Y, Nakamura T, Suzuki M. Tower climbing exercise started 3 months after ovariectomy recovers bone strength of the femur and lumbar vertebrae in aged osteopenic rats. J Bone Miner Res 2003;18:140-9.
2. Mosekilde L, Thomsen JS, Orhii PB, McCarter RJ, Meijia W, Kalu DN. Additive effect of voluntary exercise and growth hormone treatment on bone strength assessed at four different skeletal sites in an aged rat model. Bone 1999;24:71-80.
3. Mackie EJ. Osteoblast: novel roles in orchestration of skeletal architecture. Int J Biochem Cell Biol 2003;35:1301-5.
4. Robey PG. The biochemistry of bone. Biol Metab Clin North Am 1989;18:859-902.
5. Nunes IJ, Nunes VA. Doenças metabólicas do osso. Cad Tec Esc Vet UFMG 1988;3:1-66.
6. Tate MK, Adamson JR, Tami AE, Bauer TW. The osteocytes. Int J Biochem Cell Biol 2004;36:1-8.
7. Cilliname DM. The role of osteocytes in bone regulation: mineral homeostasis versus mechanoreception. J Musculoskelet Neuronal Interact 2002;2:242-4.
8. Cherian PP, Cheng B, Gu S, Sprague E, Bonewald LF, Jiang JX. Effects of mechanical strain on the function of gap junctions in osteocytes are mediated throughthe prostaglandin EP2 receptor. J Biol Chem 2003;278:43146-56.
9. Boyle WJ, Simonet WS, Lacey DL. Osteoclast differentiation and activation. Nature 2003;423:337-42.
10. Raisz LG. Physiology and pathophysiology of bone remodeling. Clin Chem 1999; 45:1353-8.
11. Bland R. Steroid hormone receptor expression and action in bone. Clin Sci 2000; 98:217-40.
12. Ribeiro AFC, Serakides R, Ocarino NM, Nunes VA. Efeito da associação hipotireoidismo-castração no osso e nas paratireóides de ratas adultas. Arq Bras Endocrinol Metab 2004;48:525-34.
13. Sinaki M. Exercise and osteoporosis. Arch Phys Med Rehabil 1989;70:220-9.
14. Hillard TC, Stevenson JC. Role of oestrogen in the development of osteoporosis. Calcif Tissue Int 1991;49:S55-9.
15. Ishida Y, Tertinegg I, Heersche JNM. Progesterone and dexamethasone stimulate proliferation and differentiation of osteoprogenitors and progenitors for adipocytes and macrophages in cell populations derived from adult rat vertebrae. J
Bone Miner Res 1996;11:921-30.
16. Tomkinson A, Gevers EF, Wit JM, Reeve J, Noble BS. The role of estrogen in thecontrol of rat osteocyte apoptosis. J Bone Miner Res 1998;13:1243-50.
17. Bilezikian JP, Raizs LG, Rodan GA. Principles of bone biology. San Diego: Academic Press, 1996;1398p.
18. Serakides R. Relação tireóide, gônadas e metabolismo ósseo em ratas adultas hipertireóideas e eutireóideas (Tese, Doutorado em Ciência Animal). Belo Horizonte, Escola de Veterinária, UFMG, 2001;90p.
19. Colin EM, Van Den Bemd GH, Van Aken M, Christakos S, De Jonge HR, Deluca HF, et al. Evidence for involved of 17 beta-estradiol in intestinal calcium absorption independent of 1,25-dihydroxyvitamin D3 level in the rat. J Bone Miner Res1999;14:57-64.
20. Liel Y, Shany S, Smirnoff P, Schwartz B. Estrogen increases 1,25-dihydroxyvitamin D receptors expression and bioresponse in the rat duodenal mucosa. Endocrinology 1999;140:280-5.
21. Schwartz B, Smirnoff P, Shany S, Sliel Y. Estrogen controls expression and bioresponse of 1,25-dihydroxyvitamin D receptors in the rat colon. Mol Cell Biochem 2000;203:87-93.
22. Williams GR, Robson H, Shalet SM. Thyroid hormone actions on cartilage and bone: interactions with other hormones at the epiphyseal plate and effects on linear growth. J Endocrinol 1998;157:391-403.
23. Serakides R, Nunes VA, Ocarino NM, Nascimento EF. Efeito da associação hipertireoidismo-castração no osso de ratas adultas. Arq Bras Endocrinol Metab2004; 48:875-84.
23. Begerow B, Pfeifer M, Pospeschill M, Scholz M,Schlotthauer T, Lazarescu A, Pollaehne W, Minne HW. (1999) Time since vertebral fracture: an important variable concerning quality of life in patients with postmenopausal osteoporosis. Osteoporos Int 10:26-33.
24. Hauer K, Specht N, Schuler M, Bartsch P, Oster P. (2002) Intensive physical training in geriatric patients after severe falls and hip surgery. Age Ageing 31:49-57.
25. Kemmler W, Lauber D, Weineck J, Hensen J, Kalender W, Engelke K. (2004) Benefits of 2 years of intense exercise on bone density, physical fitness, and blood lipids in early postmenopausal osteopenic women. Arch Intern Med 164:1084-1091
AUTORE: Simona Gruppillo Freelance e Chinesiologa di Scienze Salute e Benessere